হাইড্রোজেন বর্ণালী সিরিজ নিয়ে জানবো এখন আমরা। একটি কাচ নলে নিম্ন চাপে রাখা হাইড্রোজেন গ্যাসের ভেতর উচ্চ শক্তির বিদ্যুৎ চালনা করা হলে ঐ গ্যাসের ভেতর থেকে গোলাপী বর্ণের আলোর বিকিরণ ঘটে। এ বিকিরিত আলোকে স্পেকট্রোস্কোপের প্রিজমের মধ্য দিয়ে ফটোগ্রাফিক প্লেটে ফেললে কতগুলো সুস্পষ্ট রঙিন আলো রেখা দেখা যায়। এ উজ্জ্বল আলোক রেখাগুলোর সমাহারকে হাইড্রোজেনের রেখা বর্ণালী বা পারমাণবিক বর্ণালী বলা হয়।
আলোক সম্পর্কীয় প্লাঙ্কের তত্ত্বের সাহায্যে বিজ্ঞানী বোর হাইড্রোজেনের পারমাণবিক বর্ণালীর ব্যাখ্যায় বলেন যে, উচ্চ বিদ্যুৎ শক্তির প্রভাবে হাইড্রোজেন অণু প্রথমে পরমাণুতে পরিণত হয়। পরে হাইড্রোজেনের অসংখ্য পরমাণুর ইলেকট্রন বিভিন্ন পরিমাণে শক্তি শোষণ করে উদ্দীপিত হয়ে তাদের বিভিন্ন উচ্চ শক্তিস্তরে লাফিয়ে চলে। শক্তির উৎস সরিয়ে নিলে উদ্দীপিত ইলেকট্রনগুলো থেকে শক্তির বিকিরণ ঘটতে থাকে। ফলে ইলেকট্রনগুলো বিভিন্ন নিম্ন শক্তিস্তরে ফিরে আসে। তখন অসংখ্য H পরমাণুর বিভিন্ন উচ্চ শক্তিস্তরের ইলেকট্রন একই নিম্ন শক্তিস্তরে ফিরতে পারে। ফলে সৃষ্ট রেখা বর্ণালীর পাশাপাশি রেখাগুলো বিভিন্ন দৈর্ঘ্যের হয়।
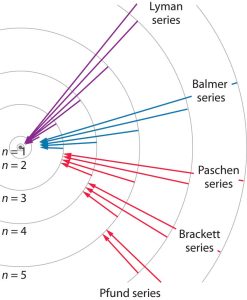
বিভিন্ন বিজ্ঞানী হাইড্রোজেন বর্ণালী সিরিজ এর চিত্র আবিষ্কার করেন, তাঁদের নামানুসারে হাইড্রোজেনের রেখা বর্ণালীর বিভিন্ন নাম আছে, যেমন- উদ্দীপিত ইলেকট্রন শক্তি হারিয়ে ১ম শক্তিস্তরে ফিরে আসলে তখন H-বর্ণালীতে যে রেখাসমূহ পাওয়া যায়, তাদের সমাহারকে লাইমেন সিরিজ বলে। তদ্রুপ উচ্চ শক্তিস্তর থেকে ইলেকট্রনসমূহ ২য়, ৩য়, ৪র্থ ও ৫ম শক্তিস্তরে ফিরে আসার ফলে সৃষ্ট বর্ণালীকে যথাক্রমে বামার সিরিজ, প্যাশ্চেন সিরিজ, ব্র্যাকেট সিরিজ, ফুন্ড সিরিজ বলা হয়। সূর্যের দৃশ্যমান আলোর মধ্যে হাইড্রোজেনের পারমাণবিক বর্ণালীর বিভিন্ন লাইন দেখা যায় এবং তাদের তরঙ্গদৈর্ঘ্য সূক্ষ্মভাবে মাপা হয়। ১৮৮৫ খ্রিস্টাব্দে জে. জে. বামার (J.J. Balmer) দেখান যে, এদের তরঙ্গ-দৈর্ঘ্যকে নিম্নের সমীকরণ দ্বারা প্রকাশ করা যায়।
